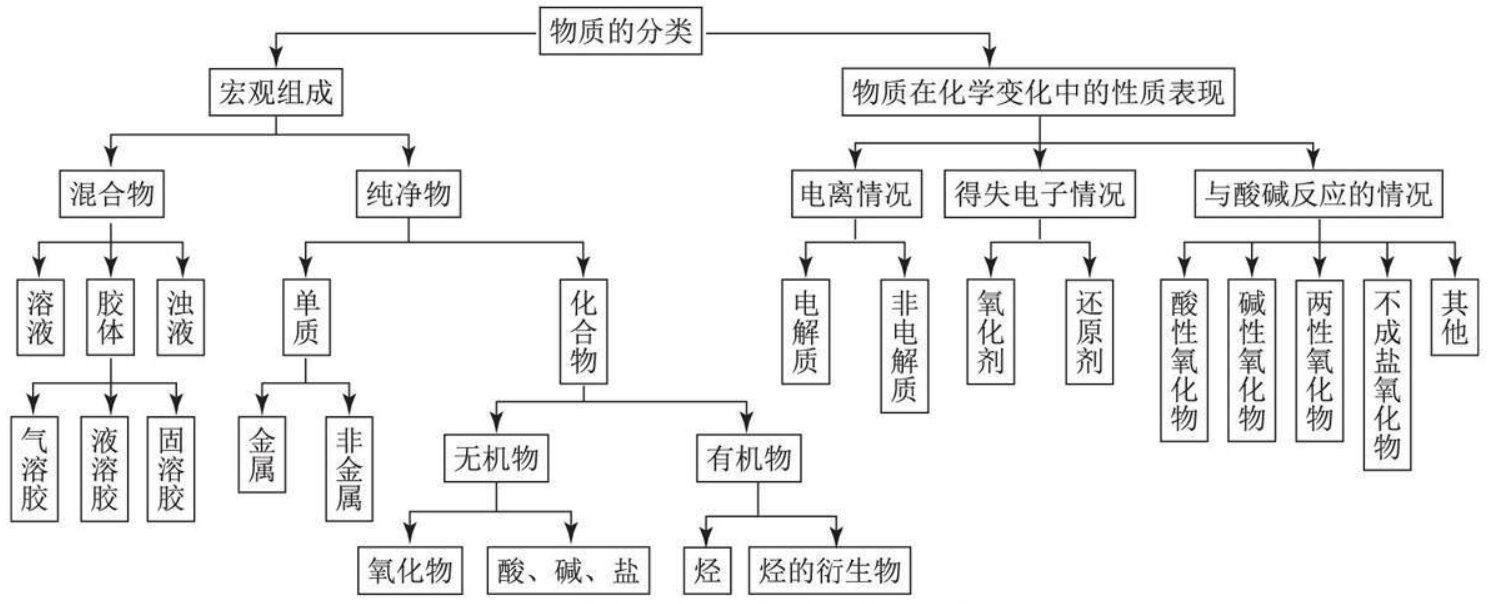
物质分类
高中会把物质分为纯净物和混合物两类,而一般写的方程式也只有纯净物,所以只用考虑纯净物之间的组合即可
这里只考虑无机方程式
单质
单质又称单纯物质、元素态物质,是由同一种元素的原子组成的纯净物
例如:氢气、硫磺、铁、碳皆是单质
元素在单质中存在时,称为该元素状态为游离态
金属单质和非金属单质
高中只用掌握这两种分离方式即可,你可以将鼠标悬浮到对应的分类上查看
简单来说带金字旁的就是金属
化合物
化合物分为酸、碱、盐、氧化物等,不想单质可以简单地通过汉字偏旁来分别,化合物的识别和分类是高中生的必备技能
比如,酸在化学中狭义的定义是:在水溶液中电离出的阳离子全部都是氢离子的化合物;广义定义是:能够接受电子对的物质
但是我认为高中生,酸、碱和盐的分类通过化学式来区分更加方便,具体如下(只考虑无机物):
酸
酸常见的化学式组成为氢离子 + 酸根离子,比如说 HCl、H2SO4,常见的酸根离子如下:
| 酸根离子名称 | 化学式 | 对应的酸 |
|---|
| 碳酸根离子 | CO32− | H2CO3 |
| 碳酸氢根离子 | HCO3− | H2CO3 |
| 硫离子 | S2− | H2S |
| 硫酸根离子 | SO42− | H2SO4 |
| 亚硫酸根离子 | SO32− | H2SO3 |
| 磷酸根离子 | PO43− | H3PO4 |
| 磷酸氢根离子 | HPO42− | H3PO4 |
| 磷酸二氢根离子 | H2PO4− | H3PO4 |
| 高锰酸根离子 | MnO4− | HMnO4 |
| 锰酸根离子 | MnO42− | HMnO4 |
| 氯离子 | Cl− | HCl |
| 氯酸根离子 | ClO3− | HClO3 |
| 亚氯酸根离子 | ClO2− | HClO2 |
| 次氯酸根离子 | ClO− | HClO |
| 高氯酸根离子 | ClO4− | HClO4 |
| 硝酸根离子 | NO3− | HNO3 |
| 亚硝酸根离子 | NO2− | HNO2 |
| 碘酸根离子 | IO3− | HIO3 |
| 硅酸根离子 | SiO32− | H2SiO3 |
| 铬酸根离子 | CrO42− | H2CrO4 |
| 重铬酸根离子 | Cr2O72− | H2Cr2O7 |
| 高铁酸根离子 | FeO42− | HFeO4 |
| 氰离子 | CN− | HCN |
| 草酸氢根离子 | HC2O4− | H2C2O4 |
| 草酸根离子 | C2O42− | H2C2O4 |
| 亚磷酸氢根离子 | HPO32− | H3PO3 |
| 铅酸根离子 | PbO32− | H2PbO3 |
| 钛酸根离子 | TiO32− | H2TiO3 |
| 三钛酸根离子 | Ti3O72− | H2Ti3O7 |
| 锗酸根离子 | GeO32− | H2GeO3 |
| 砷酸根离子 | AsO43− | H3AsO4 |
碱
碱的化学式就更简单了,由除氢外的阳离子和氢氧根离子构成,比如 NaOH 等
盐
盐是酸和碱结合的产物,化学式组成为除氢离子外的阳离子和酸根离子构成,比如 NaCl、Na2SO4、Na2CO3 等
氧化物
依旧从化学式上观察,无论是什么氧化物,都是两种元素其中一种元素是氧的二元化合物
酸性氧化物大多是非金属氧化物,碱性氧化物大多数是金属氧化物,除了以下 5 个特例:
- 非金属氧化物但不是酸性氧化物:CO、NO(高中唯二的两个不成盐氧化物)、H2O2(特殊氧化物)
- 金属氧化物但不是碱性氧化物:Mn2O7(酸性氧化物)、Fe3O4、Na2O2(特殊氧化物)、Al2O3(两性氧化物)
物质之间化学反应的规律
上文中一共列举了 7 种物质:金属单质、非金属单质、酸、碱、盐、酸性氧化物、碱性氧化物
7 种物质两两组合共有 49 种反应,除去重复、不常考和没有通性的类型,共有 12 种反应,分别如下表:
金属单质和其他物质(3 条)
| 金属单质 + 物质 | 产物 | 示例化学式 |
|---|
| 金属单质 + 非金属单质 | 盐(或金属氧化物) | 2Na+Cl2→2NaCl、2Mg+O2→2MgO |
| 金属单质 + 酸 | 盐和氢气 | Zn+H2SO4→ZnSO4+H2↑ |
| 金属单质 + 盐 | 新金属和新盐 | Cu+2AgNO3→2Ag+Cu(NO3)2 |
酸和其他物质(3 条)
| 酸 + 物质 | 产物 | 示例化学式 |
|---|
| 酸 + 碱 | 盐和水 | HCl+NaOH→NaCl+H2O |
| 酸 + 盐 | 新酸和新盐 | HCl+AgNO3→AgCl↓+HNO3 |
| 酸 + 碱性氧化物 | 盐和水 | H2SO4+MgO→MgSO4+H2O |
碱和其他物质(2 条)
| 碱 + 物质 | 产物 | 示例化学式 |
|---|
| 碱 + 盐 | 新碱和新盐 | NaOH+CuSO4→Cu(OH)2↓+Na2SO4 |
| 碱 + 酸性氧化物 | 盐和水 | NaOH+CO2→Na2CO3+H2O |
盐和其他物质(1 条)
| 盐 + 物质 | 产物 | 示例化学式 |
|---|
| 盐 + 盐 | 新盐 + 新盐 | AgNO3+NaCl→AgCl↓+NaNO3 |
酸性氧化物和其他物质(2 条)
| 酸性氧化物 + 物质 | 产物 | 示例化学式 |
|---|
| 酸性氧化物 + 水 | 酸 | SO3+H2O→H2SO4 |
| 酸性氧化物 + 碱性氧化物 | 盐 | SO3+CaO→CaSO4 |
碱性氧化物和其他物质(1 条)
| 碱性氧化物 + 物质 | 产物 | 示例化学式 |
|---|
| 碱性氧化物 + 水 | 碱 | CaO+H2O→Ca(OH)2 |
而记忆时则应该同时记住正向和反向两种情况,即 24 种类型
转化规律与元素化学
元素化学是高中最零碎的章节,记忆复杂,但是高考占比并不多。主要是:钠、镁、铝、铁、铜、硅、氯、硫、氮
现在通过上文来验证一下元素化学是否符合转化规律
以钠为例
剩下的元素你可以自行验证一下,是否符合上文的规律,然后用这种方法来记忆元素化学应该会轻松很多